- +1
普拉替尼納入優先審評,有望成為國內首個肺癌RET靶向新藥
9月8日,澎湃新聞(www.usamodel.cn)獲悉,近日,新藥普拉替尼膠囊的上市申請已獲國家藥品監督管理局受理,并被納入優先審評。
據介紹,這款新藥用于治療經含鉑化療的RET融合陽性的非小細胞肺癌。如審批順利,有望成為國內首個獲批的RET靶向治療藥物。
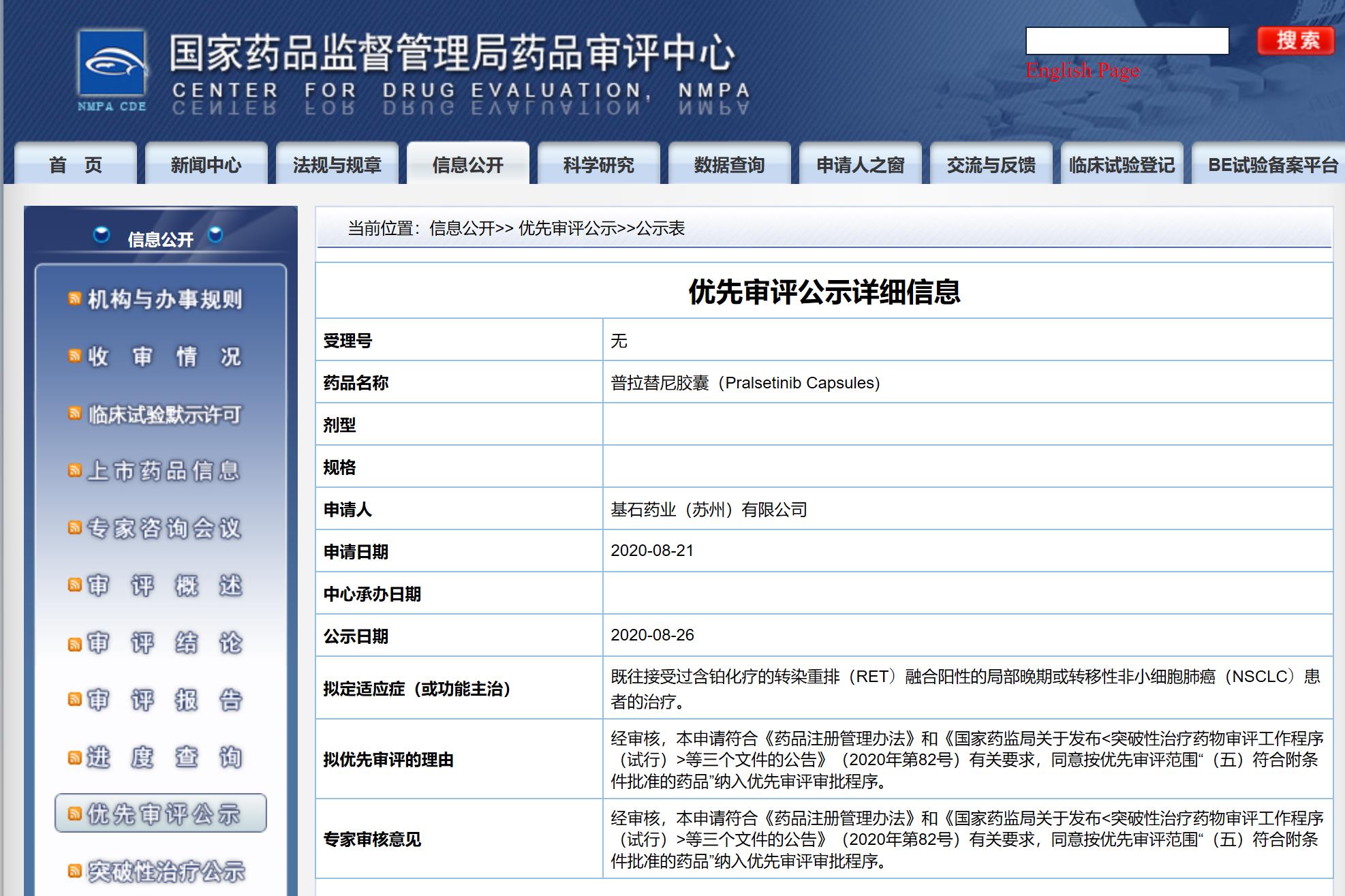
國家藥監局藥品審評中心顯示,由基石藥業申請的普拉替尼膠囊已進入優先審評程序,并于8月26日進行公示。
9月7日,港股上市公司基石藥業(蘇州)有限公司(以下簡稱“基石藥業”)宣布了該消息。
國家藥監局藥品審評中心官網顯示,基石藥業于今年8月21日向該中心申請將普拉替尼膠囊納入優先審評。8月26日,審評中心對該結果進行了公示。
公示指出,經審核,專家審核認為,該申請符合《藥品注冊管理辦法》和《國家藥監局關于發布<突破性治療藥物審評工作程序(試行)>等三個文件的公告》(2020年第82號)有關要求,同意按優先審評范圍“(五)符合附條件批準的藥品”納入優先審評審批程序。
公開資料顯示,RET基因的融合突變,近年來在部分年輕、不吸煙的肺腺癌患者中被頻頻發現,成為吸煙以外罹患肺癌不可忽視的因素之一,屬于新近發現的肺癌驅動基因。目前,對于RET融合非小細胞肺癌的一線標準治療為含鉑化療,但療效仍不理想。國內目前也尚無特異性抑制劑獲批,存在不小的臨床治療需求。
據基石藥業介紹,普拉替尼是由該公司戰略合作伙伴Blueprint Medicines Corporation開發的一款口服(每日一次)、強效和高選擇性靶向致癌性RET變異(包括可預見的耐藥突變)的在研藥物。
臨床試驗期間,在經含鉑化療的RET融合陽性的NSCLC中國患者中,普拉替尼顯示出了優越和持久的抗腫瘤活性,并且安全性及耐受性良好。這項研究結果同樣曾得到了多家媒體的關注和報道。
基石藥業首席醫學官楊建新博士介紹,基石藥業與合作伙伴從雙方達成合作到普拉替尼在國內遞交上市申請,只用了兩年時間。他表示,基石藥業將繼續推進普拉替尼在中國的研發進展,更廣泛地評估該產品在未經含鉑化療的RET融合陽性的NSCLC、甲狀腺髓樣癌和其它實體瘤患者中的療效,早日滿足這部分癌癥患者亟待解決的臨床需求。
據介紹,基石藥業成立于2015年,是一家專注于開發及商業化創新腫瘤免疫治療及精準治療藥物的生物制藥公司。





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯網新聞信息服務許可證:31120170006
增值電信業務經營許可證:滬B2-2017116
? 2014-2025 上海東方報業有限公司




