- +1
Life Med | 鐘清/魯伯塤等發表自噬溶酶體靶向降解與疾病的綜述

近日,上海交通大學醫學院、“細胞分化與凋亡”教育部重點實驗室鐘清課題組聯合復旦大學生科院魯伯塤課題組在Life Medicine發表了題為"Manipulating Autophagic Degradation in Human Diseases: from Mechanisms to Interventions"的綜述文章,文章基于選擇性自噬的機制,總結了最新最前沿利用自噬-溶酶體途徑設計新型靶向降解技術的研究進展,并展望了未來這一新型靶向降解技術在腫瘤和神經退化性疾病治療中廣泛應用前景以及待解決的關鍵科學問題。

靶向降解(targeted degradation)是近二十年來新興的一種藥物設計路線。不同于多數傳統藥物通過緊密結合靶蛋白的活性位點而抑制其功能,靶向降解藥物(degrader)嘗試利用細胞自身的降解系統選擇性消滅靶蛋白。典型的設計方案是一個雙功能的化合物:一端的基團可結合某個分子機器,另一端結合靶蛋白,通過將分子機器招募至靶蛋白引起降解效應。目前開發最為充分的是利用泛素化-蛋白酶體途徑的靶向降解路線,其代表方案為PROTAC(proteolysis-targeting chimera)。PROTAC利用的分子機器是E3連接酶,可引起靶蛋白泛素化,進而被蛋白酶體識別降解。這一策略已被成功地應用于數十種靶蛋白,并已有至少兩種PROTAC進入了臨床試驗。除蛋白酶體之外,真核細胞尚有另一個重要的降解機器,即溶酶體(lysosome)。溶酶體含有多種酸性水解酶,可降解包括蛋白、核酸、脂質在內的多種物質。近年來,構建利用溶酶體的靶向降解技術逐漸成為研究者的興趣所在。這類技術包括利用內吞-溶酶體途徑降解質膜蛋白和細胞外成分的LYTAC(lysosome-targeting chimera)等;以及利用自噬-溶酶體途徑降解細胞內成分的AUTAC(AUtophagy-TArgeting Chimera),AUTOTAC(AUTOphagy-TArgeting Chimera),ATTEC(autophagosome tethering compound)等。
自噬(autophagy),是一類將胞內物質送入溶酶體降解的途徑。其中,在多種自噬機器(autophagy machinery)的介導下,形成雙層膜的囊泡(自噬體,autophagosome)包裹底物,自噬體再與溶酶體融合的途徑,被稱為大自噬(macroautophagy),如圖1所示。具有底物選擇性的大自噬即為選擇性自噬(selective autophagy)。選擇性的實現,依賴于將分離膜(isolation membrane/phagophore,即自噬體的前體)招募至底物。這一過程由一系列底物受體(cargo receptor)與支架蛋白(scaffold protein)介導。在這篇綜述中,它們被統稱為recognition machinery,即識別機器。
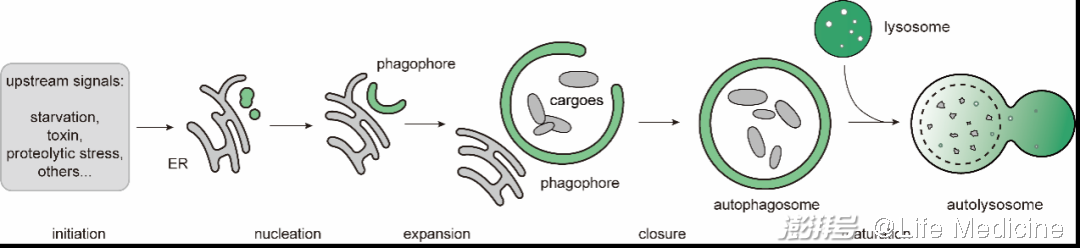
圖1(原文Figure 1A)
識別機器具有至少兩個功能:結合底物,以及招募分離膜(圖2)。在底物一端,一些識別機器結合特定的降解標簽(tag),例如泛素、N-degron或特定的糖鏈,這些標簽可以被修飾在底物表面,也可以由底物內部暴露出來;另一些底物受體可直接結合底物。在另一端,大部分底物受體都通過結合分離膜表面的mATG8蛋白而招募分離膜;除此之外,一些底物受體以及支架蛋白還可招募上游自噬機器(autophagy machinery)及它們的調節蛋白,例如ULK1復合物與TBK1等,以促進在底物所在位置(in situ,即原位)形成分離膜。
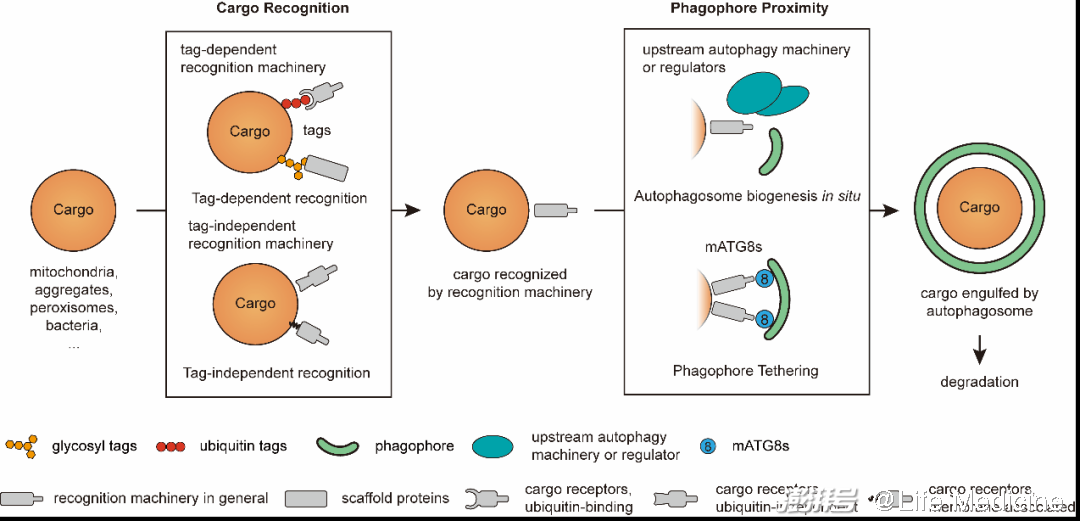
圖2(原文Figure 1B)
可見,選擇性依賴于底物、識別機器、自噬機器與分離膜之間的相互作用。若用雙功能小分子模擬這些相互作用,就有可能將靶標“導入”通向選擇性自噬的路線。基于這一思路,可以產生四種主要的自噬依賴靶向降解技術的設計策略(圖3)。
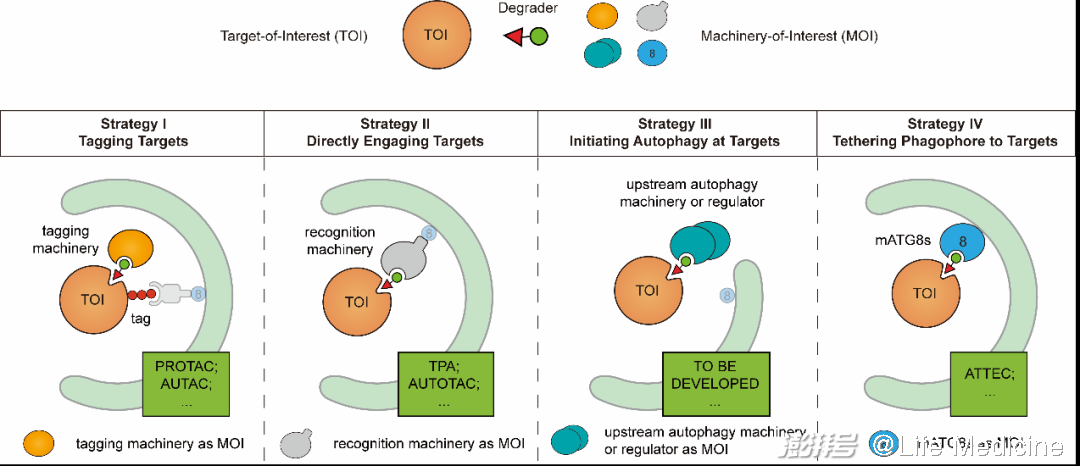
圖3(原文Figure 1C)
策略一:加降解標簽(tagging targets)。與PROTAC的原理類似,這一策略可以通過招募細胞內的修飾酶實現。這類靶向降解技術中開發相對完善的是AUTAC。這類化合物一端結合底物,另一端為一個Cys-S-cGMP類似物,結合靶標后可以引起靶標K63-多泛素化,以招募識別機器。AUTAC能夠引起線粒體以及多種可溶蛋白(Brd4、MetAP2、FKBP12)的自噬降解,不過它如何招募靶標泛素化所需的E3連接酶還不清楚。除此之外,另一些PoC實驗也給出了積極的結果。例如,使用SNIPER(selective non-genetic IAP-dependent protein eraser,PROTAC的一種類型)將IAP家族E3連接酶招募至線粒體也能成功地將線粒體泛素化,引起自噬降解。這說明PROTAC所利用的某些分子機器在特定條件下或許也可以被自噬靶向降解所利用。其他參與標記自噬底物的修飾酶,例如為蛋白加上N-Arg(一種N-degron)的ATE1,也是潛在可供利用的分子機器。
策略二:直接識別(directly engaging targets)。這一策略旨在將識別機器招募至靶標。目前已報道的識別機器包括30余種底物受體與一些支架蛋白,其中底物受體p62已經被利用開發出兩種靶向降解技術,即TPA(targeted protein autophagy)與AUTOTAC。這兩種技術都涉及一端結合底物、另一端結合p62的雙功能化合物。不同的是,TPA使用的p62配體是共價結合的,而AUTOTAC使用一個模擬N-degron結構的配體,能夠增強p62介導選擇性自噬的能力。前者成功降解了Brd4與突變Huntingtin(帶有額外poly-Q序列,會形成聚集體)。此外,也有一些PoC實驗嘗試招募p62與OPTN等識別機器到靶標。
策略三:原位引發自噬(initiating autophagy at targets)。這一策略希望招募上游自噬機器或調節蛋白,以在底物附近引發分離膜的生成。目前這一策略尚未被開發為靶向降解技術,但將ULK1、FIP200等上游自噬機器以及TBK1等調控蛋白招募至靶標的PoC實驗已經獲得了一些積極的結果。先前的研究也發現其他自噬機器,如ATG9、PI3KC3-C1、ATG12-5-16L1等,也可以被招募到選擇性自噬的底物以促進分離膜形成,因而也有被開發為靶向降解技術的潛力。
策略四:拴系分離膜(phagophore tethering of targets)。利用這一策略的靶向降解技術在靶標與分離膜之間建立聯系。由于mATG8是分離膜表面相對恒定的成分,將mATG8與底物拉在一起是目前最可靠的路線之一。利用該路線的一項典型技術是ATTEC,這類化合物可一端結合靶標,一端結合mATG8,從而使靶標被逐漸延伸的分離膜所包裹。ATTEC成功地將突變Huntingtin(帶有額外的poly-Q),Brd4以及脂滴靶向自噬降解,表現出對聚集體、可溶蛋白以及細胞器的降解能力。
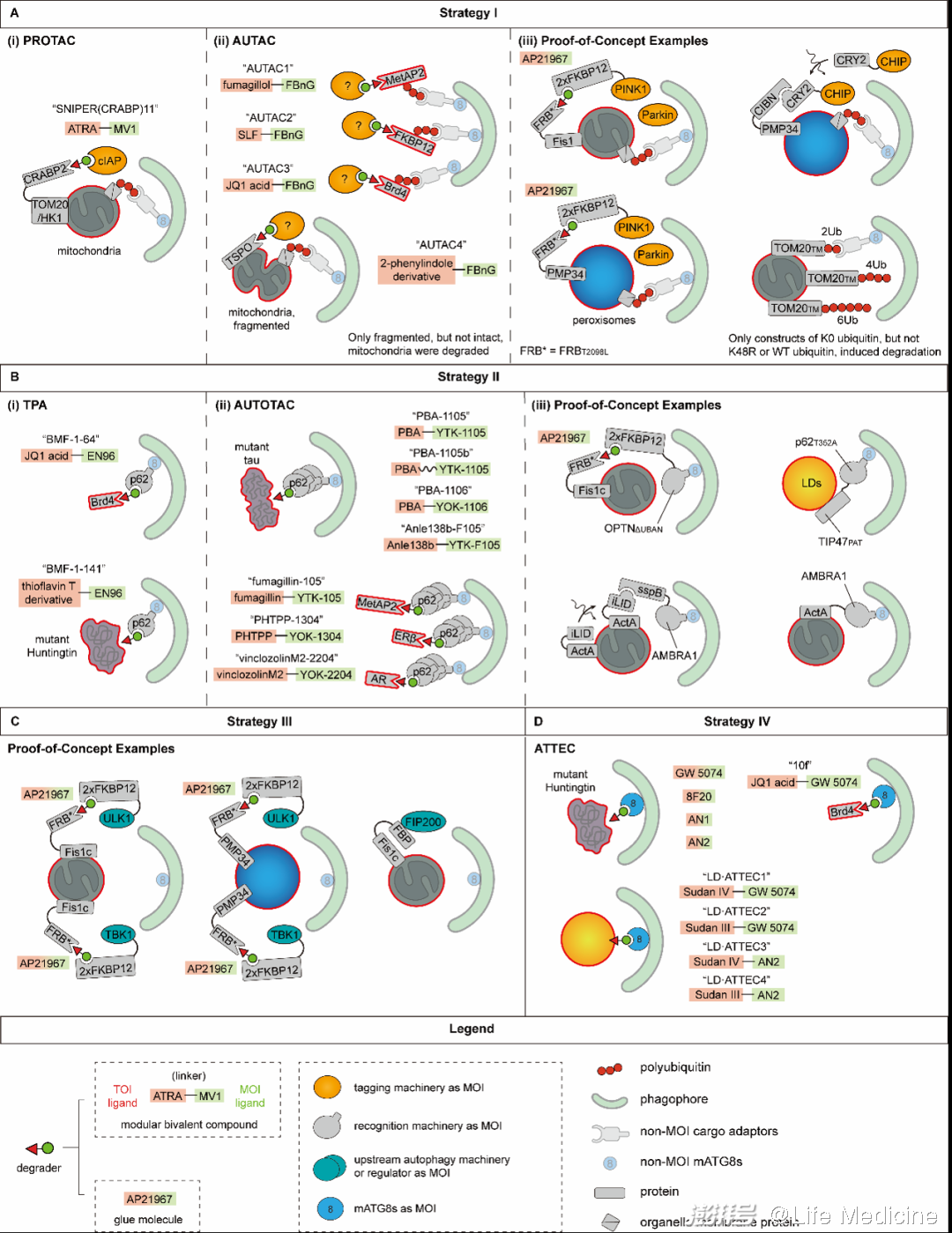
圖4(原文Figure 2,本圖篇幅所限并未包括全部案例,請參考原文)
自噬依賴靶向降解是靶向降解領域的新方向,或可被應用于多種疾病的治療。盡管已有一些分子機器被利用設計靶向降解技術,目前還有許多潛在可用的機制與分子機器未被研究;已報道的技術也有很多問題未被完全解答,降解效果也可進一步提高。理解選擇性自噬的機制與分子機器對上述過程無疑會有很大幫助。設計驗證自噬依賴靶向降解技術的過程可以從PROTAC的開發途徑得到許多啟發,但也會遇到不同于PROTAC的新問題。為此,這篇綜述討論了自噬依賴靶向降解技術可能具有的一些性質,提出了一些有待解決的問題與猜想,以及一個從確認靶標開始,開發與測試靶向降解技術的工作流程。綜上,該綜述可為開發新穎的自噬依賴靶向降解藥物提供重要的理論指導和啟發。
原文鏈接:https://doi.org/10.1093/lifemedi/lnac043
本文為澎湃號作者或機構在澎湃新聞上傳并發布,僅代表該作者或機構觀點,不代表澎湃新聞的觀點或立場,澎湃新聞僅提供信息發布平臺。申請澎湃號請用電腦訪問http://renzheng.thepaper.cn。





- 報料熱線: 021-962866
- 報料郵箱: news@thepaper.cn
互聯網新聞信息服務許可證:31120170006
增值電信業務經營許可證:滬B2-2017116
? 2014-2025 上海東方報業有限公司




